Majalah Farmasetika (V1N10-Desember 2016). Seperti yang sama-sama diketahui, obat memiliki sifat kiral. Pemisahan enansiomer untuk molekul kiral merupakan hal penting, terutama untuk industri farmasi, karena enansiomer dapat memiliki aktivitas farmakologi dan toksisitas yang berbeda.1
Apa itu obat dengan molekul kiral?
Molekul kiral adalah molekul yang mempunyai bayangan cermin tidak superimposabel (tidak dapat bertumpukan). Suatu molekul organik disebut molekul kiral jika terdapat minimal 1 atom C yang mengikat empat gugus yang berlainan.
Bencana thalidomid, reaksi senyawa kiral S-thalidomid yang tidak diinginkan
Tragedi yang sangat mungkin masih dikenang banyak orang, yang dikenal dengan “bencana thalidomid” dimana terjadi ribuan bayi lahir dengan tungkai yang terbentuk tidak sempurna karena penggunaan yang tidak tepat S-thalidomid pada wanita hamil.2
Semua peneliti kemudian berupaya menemukan metode dan tehnik untuk memisahkan obat-obat kiral sehingga diperoleh kemurnian yang tinggi. Baru pada tahun 1980, ditemukan metode-metode tersebut. Sejak saat itu, kromatografi cair kinerja tinggi (KCKT) menjadi pendekatan yang sering digunakan untuk pemisahan kiral, dan akhir-akhir ini diikuti dengan penggunaan capillary electrochromatography (CEC).3-7
Penemuan metode baru pemisahan senyawa kiral
Molecular imprinting polymer (MIP) pertama kali digunakan sebagai fase diam pemisahan kiral pada tahun 1970 oleh Wulff. Keuntungan dari MIP sebagai fase diam pemisahan kiral adalah afinititas dan selektivitas yang tinggi terhadap molekul target. Selain itu, biaya produksi dari MIP juga relatif rendah. Keuntungan ini yang kemudian meningkatkan penggunaan MIP.8
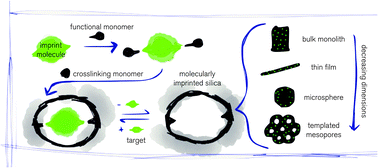
Gambar 1. Cara Pembuatan MIP.9
Seperti pada Gambar 1, MIP dibuat memlui proses pencampuran molekul template dengan monomer fungsional. Monomer fungsional mengandung gugus fungsi Y, yang kemudian akan mengalami reaksi pengikatan silang dengan pengikat silang (cross-linker)yang cocok, kemudian ruang tiga dimensi polimer akan terbentuk, dimana molekul template dikelilingi oleh monomer. Setelah itu molekul template akan dihilangkan dan meninggalkan ruang yang sama dengandengan molekul template dalam hal interaksi molekular, ukuran dan bentuk.8
Monolitik MIP telah digunakan secara ekstensif dalam KCKT untuk pemisahan kiral seperti untuk pemisahan S-ofloksasin, ketoprofen, S-citalopram.10 Matsui et al telah melakukan sintesis polimer MIP untuk fase diam pemisahan dengan metode in-situ. Dalam pembuatan MIP tersebut, senyawa template, monomer fungsional dan cross linker dicampur dalam kolom stainless steel dan dipanaskan untuk polimerisasi. Polimerisasi terjadi di dalam kolom sehingga menurunkan waktu untuk preparasi. Kolom untuk fase diam ini digunakan untuk pemisahan enansiomer turunan asam amino.
Penggunaan MIP yang berkembang untuk pemisahan kiral masih membuka banyak peluang untuk aplikasi material ini sebagai fase diam dalam KCKT maupun CEC. Usaha yang keras masih dibutuhkan untuk mendapatkan material pemisahan enansiomer berbasis MIP dengan selektivitas, efisiensi dan reprodusibilitas yang tinggi melalui pembuatan MIP dengan tehnik micro device, nanofibre dan partikel magnetik.
Referensi :
- Fanali, S. Controlling enantioselectivity in chiral capillary electrophoresis with inclusion-complexation.J. Chromatogr. A 1997, 792, 227–267
- Kim, J.H.; Scialli, A.R. Thalidomide: The tragedy of birth defects and the effective treatment of disease.Toxicol. Sci. 2011, 122, 1–6
- Okamoto, Y.; Ikai, T. Chiral HPLC for efficient resolution of enantiomers. Chem. Soc. Rev. 2008,37,2593–2608.
- Ward, T.J.; Ward, K.D. Chiral separations: Fundamental review 2010. Anal. Chem. 2010, 82, 4712–4722.
- Huang, Y.P.; Liu, Z.S.; Zheng, C.; Gao, R.Y. Recent developments of molecularly imprinted polymer in CEC. Electrophoresis 2009, 30, 155–162.
- Al-Othman, Z.A.; Al-Warthan, A.; Ali, I. Advances in enantiomeric resolution on monolithic chiralstationary phases in liquid chromatography and electrochromatography. J. Sep. Sci. 2014,37,1033–1057.
- Iacob, B.C.; Bodoki, E.; Oprean, R. Recent advances in capillary electrochromatography using molecularly imprinted polymers. Electrophoresis 2014, 35, 2722–2732.
- Vasapollo, G.; Sole, R.D.; Mergola, L.; Lazzoi, M.R.; Scardino, A.; Scorrano, S.; Mele, G.
Molecularly imprinted polymers: Present and future prospective. Int. J. Mol. Sci. 2011, 12, 5908–5945. - Lofgreen, J.E.; Ozin, G.A. Controlling morphology and porosity to improve performance of molecularly imprinted sol-gel silica. Chem. Soc. Rev. 2014, 43, 911–933
- Dong, H.; Zheng, M.; Ou, Y.; Zhang, C.; Liu, L.; Li, J.; Yang, X. A chiral stationary phase coated bysurface molecularly imprinted polymer for separating 1, 10-binaphthalene-2, 20 diamine enantiomer by high performance liquid chromatography. J. Chromatogr. A 2015, 1376, 172–176.
Artikel Majalah Farmasetika ini termasuk kedalam artikel edisi khusus yang akan diterbitkan di http://jurnal.unpad.ac.id/farmasetika
 Info Farmasi Terkini Berbasis Ilmiah dan Praktis Majalah Farmasi Online Pertama di Indonesia
Info Farmasi Terkini Berbasis Ilmiah dan Praktis Majalah Farmasi Online Pertama di Indonesia

